| Small Intestine IIeum | Подвздошная кишка тонкого кишечника |
| Salmonella | Сальмонелла |
| SFB | СНБ |
| Segmented Filamentous Bacteria (SFB) | Сегментоядерные нитчатые бактерии (СНБ) |
| M cell | M-клетки |
| CGRP | CGRP |
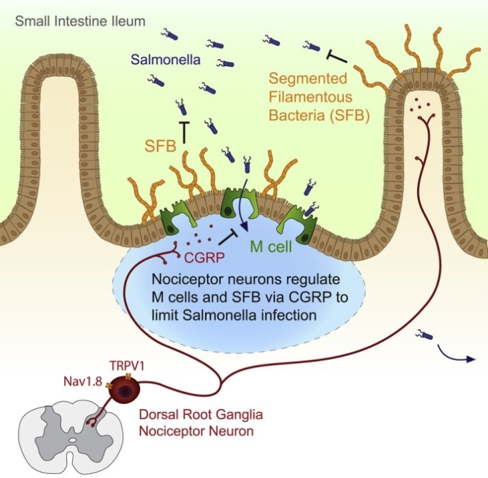
| Nociceptor neurons regulate M cells and SFB via CGRP to limit Salmonella infection | Ноцицепторные нейроны регулируют М-клетки и СНБ посредством CGRP (ген-кальцитонинового пептида) для ограничения инфицирования сальмонеллой. |
| Nav1.8 | Nav1.8 |
| TRVP1 | TRVP1 |
| Dorsal Root Ganglia Nociceptor Neuron | Нейрон ноцицептивных волокон в ганглиях дорсальных корешков |
| Graphical abstract. Credit: Cell (2019). DOI:10.1016/j.cell.2019.11.014 | Иллюстрация. Источник: «Клетка» (Cell) — 2019 г. ИЦО: 10.1016/j.cell.2019.11.014 |
Согласно исследованию Медицинского колледжа Вейла Корнелла, чувствительные к боли нейроны защищают кишечник от воспаления и связанного с ним повреждения тканей посредством регулировки микробного сообщества, населяющего кишечник.
Исследователями, чей отчет опубликован в журнале «Клетка» (Cell) от 14 октября, в рамках доклинической модели было обнаружено, что чувствительные к боли нейроны кишечника выделяют молекулу, называемую субстанцией P, которая, вероятно, защищает кишечник от воспаления, а также связанного с ним повреждения тканей посредством увеличения популяции полезных микробов в кишечнике. Исследователями также было обнаружено, что у лиц с воспалительным заболеванием кишечника (ВЗК) количество таких чувствительных к боли нервов уменьшается, а в их генах, ответственных за передачу болевого сигнала, наблюдаются значительные нарушения.
«Эти результаты меняют наши представления о хронических воспалительных заболеваниях и открывают совершенно новый подход к терапевтическому вмешательству», — заявляет ведущий автор исследования доктор Дэвид Артис, директор Института исследований воспалительных заболеваний кишечника Джилл Робертс, директор Центра питания и воспаления Фридмана и профессор иммунологии Майкла Корса в Медицинском колледже Вейла Корнелла.
Первый автор исследования, доктор Вэнь Чжан, научный сотрудник лаборатории доктора Артиса, добавляет, что «определение ранее неизвестной сенсорной функции этих конкретных нейронов, влияющих на микробиоту, открывает новый уровень понимания взаимодействий между организмом-хозяином и микробиотой».
ВЗК включает два различных заболевания (болезнь Крона и язвенный колит) и, предположительно, является проблемой для нескольких миллионов американцев.Как правило, лечение ВЗК подразумевает использование препаратов, непосредственно воздействующих на элементы иммунной системы. В настоящее время ученые понимают, что кишечные бактерии и прочие микробы также позволяют регулировать воспаление кишечника.
Как показали в последние годы лаборатория доктора Артиса и другие лаборатории, нервная система, «подключенная» к большинству органов, выступает в качестве еще одного мощного регулятора иммунной системы на барьерных поверхностях тела. В своем новом исследовании доктор Артис со своей командой конкретно изучал болевые нейроны, которые иннервируют (т. е. распространяют свои нервные окончания) в кишечник.
Такие иннервирующие кишечник болевые нейроны, тела которых располагаются в нижней части позвоночника, экспрессируют поверхностный белок, называемый TRPV1, выступающий в качестве рецептора для связанных с болью сигналов. TRPV1 можно активировать, например, высокими температурами, кислотой и капсаицином (соединением перца чили), и мозг переводит эту активацию в чувство жгучей боли. Исследователями было обнаружено, что подавление рецепторов TRPV1 в кишечных нервах или удаление нейронов, экспрессирующих TRPV1, обуславливало развитие гораздо более сильного воспаления и повреждения тканей на моделях мышей с ВЗК, тогда как активация этих рецепторов оказывала защитный эффект.
Исследователи отмечают, что обострение воспаления и повреждение тканей у мышей с блокировкой TRPV1 были связаны с изменениями в относительных популяциях различных видов кишечных бактерий.
При трансплантации такой измененной бактериальной популяции здоровым мышам она вызывала идентичное ухудшение восприимчивости к воспалению и повреждению. Напротив, лечение антибиотиками широкого спектра действия потенциально позволяет обратить эту восприимчивость даже у мышей с блокировкой TRPV1. Такой результат доказывает, что нервы, экспрессирующие TRPV1, защищают кишечник, главным образом, посредством поддержания здоровой популяции кишечных микробов.
Ученые обнаружили убедительные доказательства того, что большая часть этого влияния на микробы со стороны нервов, экспрессирующих TRPV1, обусловлена молекулой, выделяемой нервами и называемой субстанцией P, которая, как было показано, может сама по себе обратить вспять большинство негативных эффектов блокирования TRPV1. В рамках экспериментов также было продемонстрировано, что передача сигналов между нейронами и микробами была двусторонней: так, некоторые виды бактерий могли возбуждать нервы, экспрессирующие TRPV1, для активизации выработки субстанции P. Для подтверждения применимости этих результатов к человеку исследователями были рассмотрены ткани кишечника пациентов с ВЗК и обнаружена аномальная активность генов TRPV1 и субстанции P, а также меньшее количество признаков нервов TRPV1 в целом.
«У этих пациентов были повреждены чувствительные к боли нервы, что могло способствовать развитию у них хронического воспаления», — заявляет доктор Чжан.
Как именно субстанция Р оказывает влияние на популяцию кишечных микробов и как эти микробы «отвечают» на него, — вот вопросы, на которые исследователи пытаются ответить в настоящее время в рамках текущих исследований. Тем не менее полученные результаты демонстрируют, что противовоспалительные препараты следующего поколения, предназначенные для лечения ВЗК и прочих заболеваний, могут представлять собой соединения, воздействующие на нервную систему.
«Многие современные противовоспалительные препараты эффективны лишь у ряда пациентов, и фармацевтические компании действительно не знают почему, — заявляет доктор Артис. — Вероятно, так происходит потому, что когда речь шла о хроническом воспалении, мы наблюдали только часть картины. Теперь же, внимание начинает привлекать остальная часть, в том числе и роль нервной системы».
Дополнительная информация: Wen Zhang et al, Gutinnervating nociceptors regulate the intestinal microbiota to promote tissue protection, Cell (2022). // Вэнь Чжан и соавт. Ноцицепторы, иннервирующие кишечник, регулируют кишечную микробиоту и способствуют защите тканей. Ж. «Клетка». — 2022. ИЦО: 10.1016/j.cell.2022.09.008 Предоставлено Медицинским колледжем Вейла Корнелла
Цитирование АРА: Защита кишечника от воспаления благодаря чувствительным к боли нейронам (14 октября 2022 г.). Статья получена: 22 ноября 2022 г. по ссылке: https://medicalxpress.com/news/2022-10-pain-sensing-gut-neurons- inflammation.html
© Все права защищены 2025
Раздел «Врач» предназначен исключительно для медицинских специалистов. Информация, представленная в данном разделе, носит специализированный характер и предназначена для профессионального использования в медицинской практике.
Выполните вход или зарегистрируйтесь
Отправляя сообщение вы соглашаетесь с Политикой обработки персональных данных и Политикой конфиденциальности